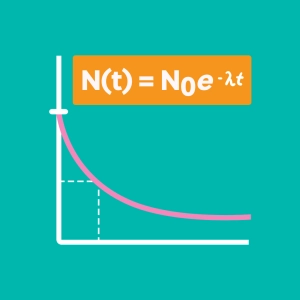
PV = NkT
PV = NkT
Objectifs d’apprentissage
- Décrire la relation entre les collisions des particules contre la paroi et la pression.
- Déterminer comment la variation d'une variable parmi P, V, N et T influence les propriétés du gaz.
- Introduire quelques concepts de la théorie cinétique des gaz.
- Rappeler le rôle fondamental de la constante d'Avogadro.
Cette simulation offre une perspective unique sur le monde microscopique qui sous-tend le comportement macroscopique des gaz. Par exemple, il est possible d'augmenter le nombre de molécules (N) ou de moles (n) tout en maintenant le volume et la température constants, et d'observer directement comment un plus grand nombre de particules engendre des collisions plus fréquentes avec les parois, augmentant ainsi la pression.
L'interprétation moléculaire de la pression devient alors profondément intuitive. De même, cette simulation fait le lien entre l'énergie cinétique des molécules et la température. La température n'est pas simplement une valeur affichée par un thermomètre, mais une mesure de l'agitation moléculaire. En manipulant tous les paramètres, il est possible d'établir un lien entre le modèle particulaire et l'équation des gaz parfaits PV = nRT. Cette perspective multi-échelle – des molécules individuelles aux grandeurs mesurables – est essentielle pour développer une compréhension conceptuelle des grandeurs d'état chimique.

Découvrez EduMedia gratuitement
L’encyclopédie intéractive qui donne vie aux sciences et aux maths en classe.
Plus de 1000 ressources