 Décroissance radioactive
Décroissance radioactive
Objectifs d’apprentissage
- Comprendre le caractère aléatoire de la désintégration radioactive ;
- Savoir définir la demi-vie pour trois radionucléides représentatifs ;
- Relier le Becquerel au processus de désintegration ;
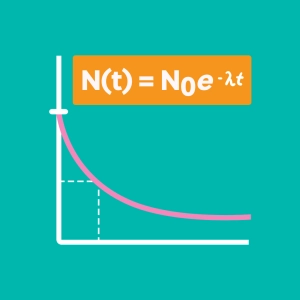
- Visualiser l'évolution temporelle de la loi de décroissance exponentielle.
Le noyau d'un atome est caractérisé par son nombre de protons (Numéro atomique Z), son nombre de nucléons (nombre de masse A). Un atome d'une même espèce chimique peut contenir un nombre différent de nucléons A, c'est à dire un nombre différent de neutrons (N = A - Z). Les atomes dont le nombre de neutrons diffère constituent les isotopes de cet atome. Les isotopes d'un atome possèdent tous les mêmes propriétés chimiques (même nombre Z) et demeurent sauf exception en proportion constante dans la nature.
Un noyau est stable quand la force nucléaire compense la force de répulsion électrique entre les protons chargés positivement. Certains noyaux sont instables. Ils se transforment naturellement en libérant de l'énergie (rayonnement) et en générant de nouveaux noyaux qui peuvent être à leur tour stables ou instables. Cette désintégration est aléatoire, elle dépend de la nature de l'élément : c'est la radioactivité.
Cette simulation permet d'aborder de nombreuses notions relatives à la décroissance radioactive: datation, processus aléatoire, durée de vie.

Découvrez EduMedia gratuitement
L’encyclopédie intéractive qui donne vie aux sciences et aux maths en classe.
Plus de 1000 ressources





