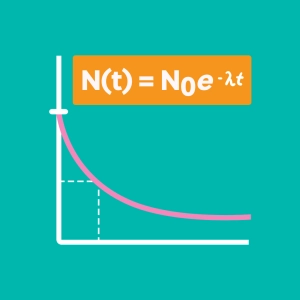
pV = NkT
pV = NkT
Lernziele
- Die Beziehung zwischen Teilchen-Wand-Kollisionen und Druck beschreiben.
- Ermitteln, wie sich die Änderung einer Variablen (P, V, N oder T) auf die Gaseigenschaften auswirkt.
- Einige Konzepte der kinetischen Gastheorie einführen.
- Die fundamentale Bedeutung der Avogadro-Konstante verdeutlichen.
Neben der Überprüfung mathematischer Proportionen ermöglicht die Simulation einen tiefen Einblick in die mikroskopische Welt, die dem makroskopischen Gasverhalten zugrunde liegt. So lässt sich beispielsweise die Anzahl der Moleküle (N) oder Mol (n) erhöhen, während das Volumen und die Temperatur konstant bleiben. Dabei kann direkt beobachtet werden, wie eine größere Anzahl von Teilchen zu häufigeren Wandkollisionen und somit zu einem höheren Druck führt.
Dies macht die molekulare Interpretation des Drucks besonders anschaulich. Lehrkräfte können Schülerinnen und Schüler außerdem dabei unterstützen, die kinetische Energie der Moleküle mit der Temperatur in Verbindung zu bringen. Dadurch wird ihnen verdeutlicht, dass Temperatur nicht nur ein Messwert auf einem Thermometer ist, sondern ein Maß für die molekulare Bewegung. Durch das Experimentieren mit allen Parametern können die Schülerinnen und Schüler eine Verbindung zwischen dem Teilchenmodell und der idealen Gasgleichung PV = nRT herstellen. Diese multiskalige Perspektive – von einzelnen Molekülen bis hin zu messbaren Größen – ist essenziell für die Entwicklung eines nachhaltigen konzeptuellen Verständnisses.

EduMedia kostenlos entdecken
Die interaktive Enzyklopädie, die Wissenschaft und Mathematik im Unterricht zum Leben erweckt.
Mehr als 1000 Ressourcen