Tabla de nucleidos
Tabla de nucleidos
Objetivos de aprendizaje
- Identificar todos los isótopos de todos los elementos conocidos.
- Comprender los criterios de inestabilidad y los diferentes tipos de desintegración radiactiva.
- Definir las cadenas de desintegración y posibles ancestros de un elemento estable.
- Introducir la vida media como criterio de estabilidad.
El número atómico Z de un elemento representa el número de protones presentes en su núcleo.
- Z = 6 para carbono
- Z = 8 para oxígeno
- Z = 20 para calcio
- Z = 92 para el uranio
El núcleo también contiene neutrones. Dos átomos pueden tener el mismo número de protones (mismo Z), pero no el mismo número de neutrones (N). El número de masa A de un elemento es el número de nucleones presentes en su núcleo, por lo que A = N + Z. Dos átomos que tienen el mismo Z pero no el mismo A son isótopos del mismo elemento químico.
Ejemplo: Los átomos de carbono que conocemos son en su mayoría átomos con 6 protones (Z = 6) y 6 neutrones (A = 12), pero hay una proporción muy pequeña de carbono con 6 protones (Z = 6) y 8 neutrones (A = 14). Este "carbono 14" es un isótopo de carbono.
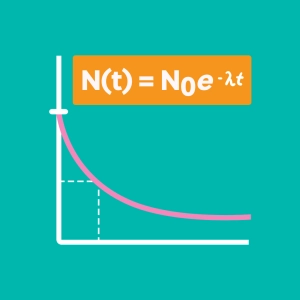
Un átomo es estable cuando el número de neutrones se aproxima al número de protones. Si se produce una brecha demasiado grande, el núcleo se vuelve inestable y puede sufrir uno o más decaimientos radiactivos para recuperar la estabilidad.
Los cuadros negros en el mapa de nucleidos en la animación representan núcleos estables. Cualquier átomo ubicado fuera de esta zona es inestable y sufrirá desintegraciones o decaimientos para llegar a esta zona.
La radiactividad es un fenómeno natural en el que el núcleo de un átomo inestable se desintegra en otro elemento más estable. Durante esta desintegración se emiten partículas y/o radiaciones de alta energía. También hablamos de radiaciones ionizantes ya que estas radiaciones tienen la capacidad de crear iones cuando penetran en la materia. Conocemos muchas aplicaciones de estas radiaciones, ya sea en medicina (medicina nuclear), datación, producción de energía, militar.
Gracias a la AIEA (Agencia Internacional de Energía Atómica) por su valiosa fuente de información que es el portal de recursos de información NUCLEUS de la AIEA. Su API (Livechart Data Download API) fue de gran ayuda para desarrollar esta animación educativa.

Descubra EduMedia gratuitamente
La enciclopedia interactiva que da vida a las ciencias y las matemáticas en el aula.
Más de 1000 recursos